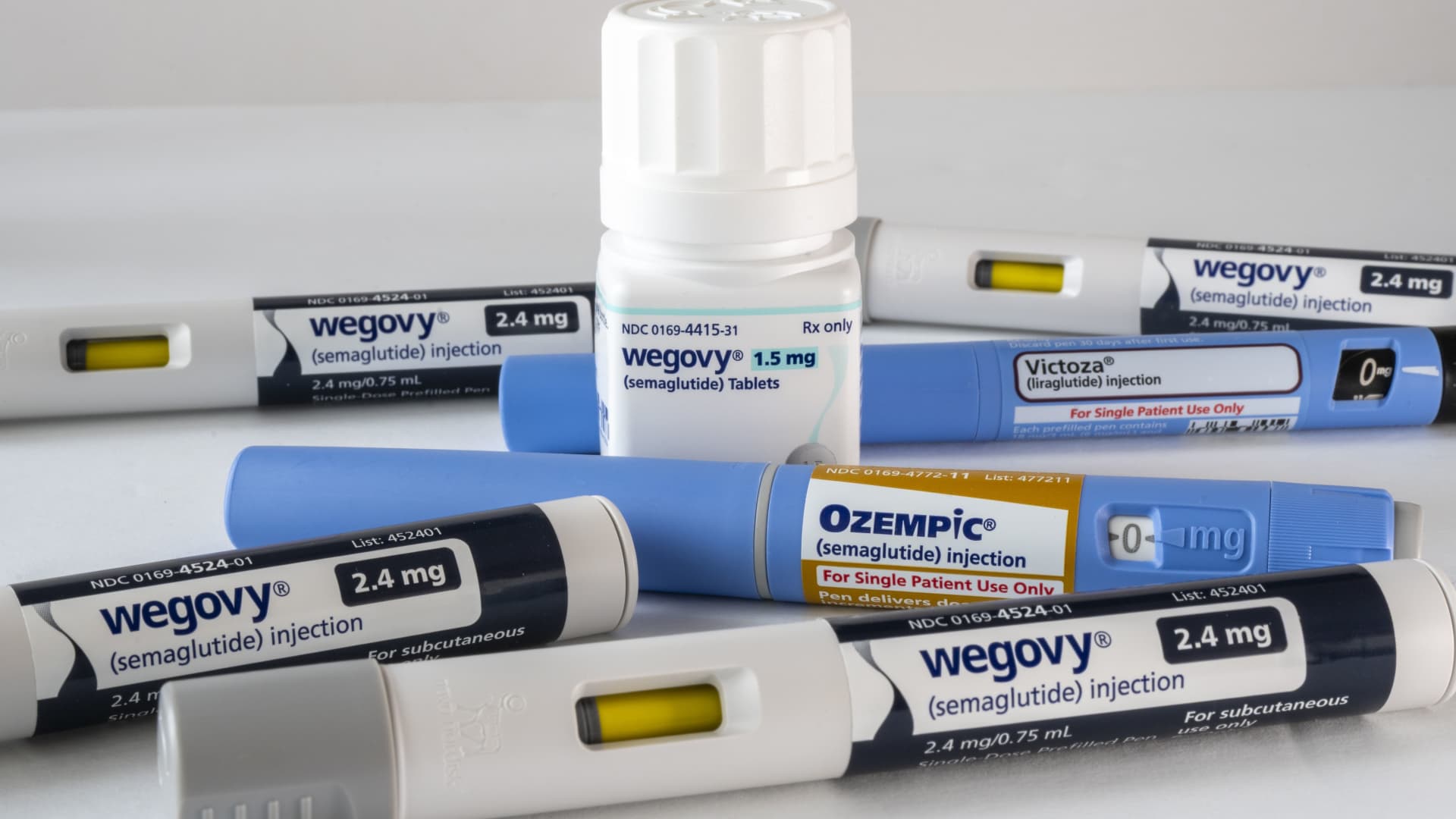
Wegovy franchit une étape majeure au Royaume-Uni : une recommandation officielle pour la prévention cardiovasculaire
Le groupe pharmaceutique danois Novo Nordisk a vu son action progresser après une décision importante de l’autorité sanitaire britannique. Le National Institute for Health and Care Excellence (NICE) a en effet recommandé l’utilisation du médicament amaigrissant Wegovy (sémaglutide) pour prévenir les crises cardiaques et les accidents vasculaires cérébraux (AVC) chez les patients à haut risque. Il s’agit de la première recommandation officielle au Royaume-Uni soutenant l’usage d’un agoniste du récepteur du GLP-1 (GLP-1 RA) dans cette indication, élargissant ainsi considérablement son accès au sein du National Health Service (NHS).
Quelle est la portée de cette recommandation du NICE ?
Jusqu’ici, l’accès à Wegovy pour la prévention cardiovasculaire au Royaume-Uni était très limité, nécessitant un financement privé. La nouvelle directive du NICE change la donne en intégrant le sémaglutide (principe actif de Wegovy et d’Ozempic) dans le parcours de soins standard pour une population spécifique.
Concrètement, le NICE recommande le sémaglutide en complément des traitements cardiovasculaires existants pour les adultes ayant déjà subi un événement cardiovasculaire majeur (crise cardiaque, AVC ou artériopathie oblitérante des membres inférieurs) et présentant un indice de masse corporelle (IMC) d’au moins 27. L’organisme estime qu’environ 1,2 million de personnes au Royaume-Uni pourraient répondre à ces critères et bénéficier potentiellement de ce traitement préventif.
Des données cliniques solides à l’appui
Cette recommandation s’appuie sur les résultats robustes de l’essai clinique de phase 3 SELECT, publié dans le New England Journal of Medicine. Les données ont montré que les patients traités par une dose de 2,4 mg de sémaglutide présentaient une réduction de 20 % du risque d’événement cardiovasculaire majeur (décès cardiovasculaire, infarctus non mortel ou AVC non mortel) par rapport au placebo, en plus des soins standards.
« Ensemble, ces décisions reflètent le nombre croissant de preuves selon lesquelles cette classe de médicaments offre des avantages allant au-delà de la perte de poids », a souligné le NICE dans son communiqué. Cette double approbation – perte de poids et protection cardiovasculaire – positionne le sémaglutide comme un outil thérapeutique aux bénéfices multiples pour les patients vivant avec l’obésité et des comorbidités.
Un impact significatif sur le système de santé et le marché
Pour le NHS, l’intégration de Wegovy dans le parcours de soins cardiovasculaires représente une évolution notable. Les maladies cardiaques et circulatoires étant l’une des principales causes de décès prématurés en Angleterre, et près d’un adulte sur quatre au Royaume-Uni vivant avec l’obésité selon le NHS, l’impact potentiel en santé publique est considérable.
Sur le plan boursier, l’action Novo Nordisk a initialement bondi de près de 4 % à l’annonce, avant de terminer en hausse de 1,7 % en fin de séance matinale à Copenhague. Cette volatilité reflète l’importance stratégique de ce nouveau marché pour le laboratoire danois, qui fait face à une concurrence accrue, notamment de la part d’Eli Lilly et de son traitement Zepbound (tirzepatide), perçu comme plus efficace pour la perte de poids.
Le contexte concurrentiel et les défis de Novo Nordisk
Cette recommandation arrive alors que Novo Nordisk navigue dans un environnement de plus en plus concurrentiel et sous pression. L’entreprise a perdu des parts de marché aux États-Unis face à Lilly, dont les médicaments induisent une perte de poids plus importante aux doses approuvées. Parallèlement, elle subit des pressions politiques sur les prix aux États-Unis, son plus grand marché, ainsi que la menace de la concurrence des génériques, notamment en Inde.
Pour tenter de riposter, Novo a lancé en 2026 une version orale de Wegovy – une première dans la classe des GLP-1 RA pour la perte de poids – et une dose plus élevée de Wegovy pour mieux rivaliser avec Zepbound. La recommandation du NICE pour la cardiologie offre ainsi un nouveau levier de croissance et de différenciation thérapeutique.
Perspectives et réactions des acteurs
Pour les cliniciens anglais, cette recommandation offre désormais une option thérapeutique « rentable » et prouvée pour une population à très haut risque. « Cela signifie que les cliniciens en Angleterre ont désormais accès à un traitement supplémentaire que le NICE a jugé rentable, le premier et le seul agoniste des récepteurs GLP-1 dont il a été prouvé qu’il réduisait le risque de crise cardiaque, d’accident vasculaire cérébral ou de décès cardiovasculaire dans cette population », a commenté Sebnem Avsar Tuna, directrice générale de Novo Nordisk UK.
Cette décision britannique pourrait servir de modèle à d’autres systèmes de santé nationaux examinant le rapport coût-efficacité des traitements GLP-1 RA au-delà du diabète et de l’obésité simple. Elle souligne également la nécessité continue d’évaluer l’impact à long terme de ces médicaments sur la morbidité et la mortalité cardiovasculaire dans des populations du monde réel.
- Source principale : Recommandation du NICE (2024) et communiqué de presse de Novo Nordisk UK.
- Données cliniques : Étude SELECT (NEJM, 2023) démontrant une réduction de 20 % du risque cardiovasculaire majeur avec le sémaglutide 2,4 mg.
- Statistiques sanitaires : NHS England sur l’obésité et les maladies cardiovasculaires.